临床医生通常会根据患者肿瘤的临床病理特征(肿瘤的大小,淋巴结状态,激素受体状态和HER2表达状态)判断患者预后并制定合理的治疗方案(化疗、放疗、内分泌治疗、靶向治疗等)。与传统的临床病理指标相比,多基因检测可以为患者提供个体化的治疗方案和预后信息,避免某些患者过度治疗或治疗不足的情况。下面,本文将重点解读3篇SABCS大会中关于70基因MammaPrint分子检测的最新研究结果。
MammaPrint低风险但非极低风险患者可从5年内分泌延长治疗中显著获益
GS5-10 Utility of the 70-gene MammaPrint test for prediction of extended endocrine therapy benefit in patients with early-stage breast cancer in the IDEAL Trial
研究背景
对于所有早期ER阳性浸润性乳腺癌的患者,超过5年的延长辅助内分泌治疗是一种选择。
2021年ASCO大会上报告的NSABP B42 研究结果显示:MammaPrint低风险但非极低风险肿瘤患者可从内分泌延长治疗(EET) 中显著获益。
IDEAL研究显示,绝经后激素受体阳性(HR+)的乳腺癌患者,在标准的5年内分泌治疗后,使用来曲唑进行5年内分泌延长治疗与2.5年延长相比DFS、DMFS、OS无显著延长。

本研究旨在探索在IDEAL研究中MammaPrint检测对预测早期乳腺癌患者延长内分泌治疗疗效获益的作用。
研究概览
患者情况:515名在随机化后2.5年未出现疾病进展或死亡的患者纳入研究分析,根据MammaPrint检测结果分为较高风险和较低风险,低风险进一步分为极低(Ultra-Low)风险或非极低(non-Ultralow)风险。中位随访时间为10.2年。

主要终点:远处复发时间(DR,随机分组后2.5年至发生远处复发的时间) ;
次要终点:无复发间期(RFI,随机化后2.5年到发生局部、区域、远处复发的时间);无乳腺癌复发间期(BCFI,随机化后2.5年至局部、区域或远处复发或对侧乳腺癌作为首次事件的时间)。
研究结果
在MammaPrint低风险患者中, 接受5年EET治疗与2.5年EET相比,DR(HR=0.42)、 RFI(HR=0.43)均显著增加。然而MammaPrint高风险患者未显示出能从5年的EET中显著获益,可能与早期复发风险(5年以内)较高和对内分泌治疗的敏感性降低有关。

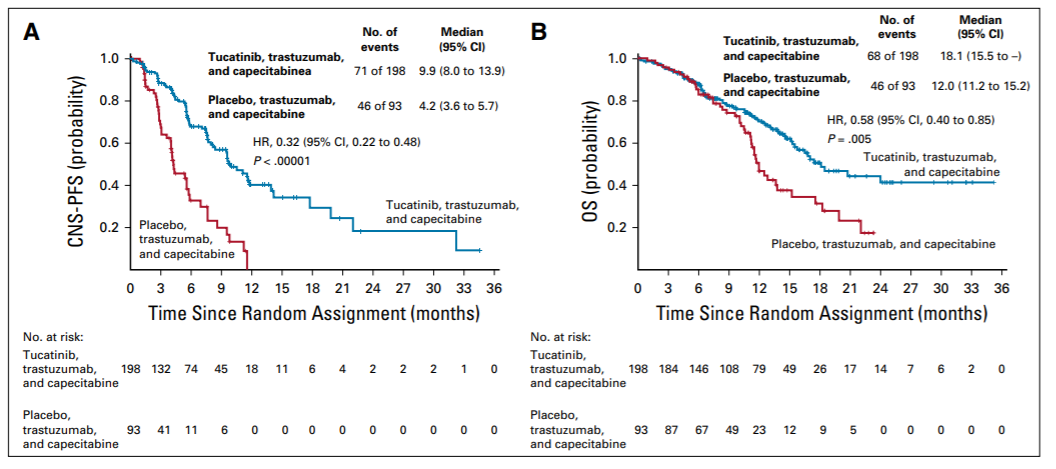
进一步细分人群发现,MammaPrint低风险但非极低风险患者中,5年EET给患者带来的获益更加明显,接受5年EET治疗与2.5年EET相比, DR、 RFI和BCFI均显著增加,10年DR、RFI、BCFI绝对获益分别为10.1%(HR = 0.32)、11.7%(HR = 0.35)和9.7%(HR = 0.48),使DR风险降低68%,RFI风险降低63%以及BCFI风险降低52%。
研究结论
在IDEAL试验中,MammaPrint低风险但非极低风险患者从5年内分泌延长治疗中获益明显,这与之前NSABP-B42试验结果一致(5年EET vs 安慰剂)。IDEAL和NSABP-B42研究的意义在于提示MammaPrint风险评估可以预测EET获益、 MammaPrint高风险患者可以避免EET过度治疗、 MammaPrint低风险但非极低风险患者可以从EET中获益。

10年随访数据出炉!
MammaPrint检测助力
早期乳腺癌精准的内分泌治疗
P4-02-20 Utility of the 70-gene signature and 10 year follow up in patients with early-stage breast cancer in a single institution study
研究背景
临床医生通常使用基因组检测来指导早期乳腺癌(EBC)的治疗。70基因MammaPrint检测(MP)不仅可以用于指导淋巴结阴性或淋巴结阳性的EBC患者化疗决策,也可用于指导内分泌治疗(ET)的降级。
本研究报告了EBC患者经MammaPrint评估的远处转移风险和10年预后分析结果。
研究概览
纳入患者:回顾性分析2005年至2008年间纳入的259名诊断为EBC并接受MP检测的女性患者。中位随访时间为13.1年。
风险分层:使用MP对未经治疗的EBC患者进行远处转移的风险评估。肿瘤分为高风险或低风险(LR)。低风险进一步分为低风险但非极低风险(LNUL)和极低风险(UL)。
研究终点:10年无远处转移间期(DMFI)和10年乳腺癌特异生存期(BCSS)。
研究结果
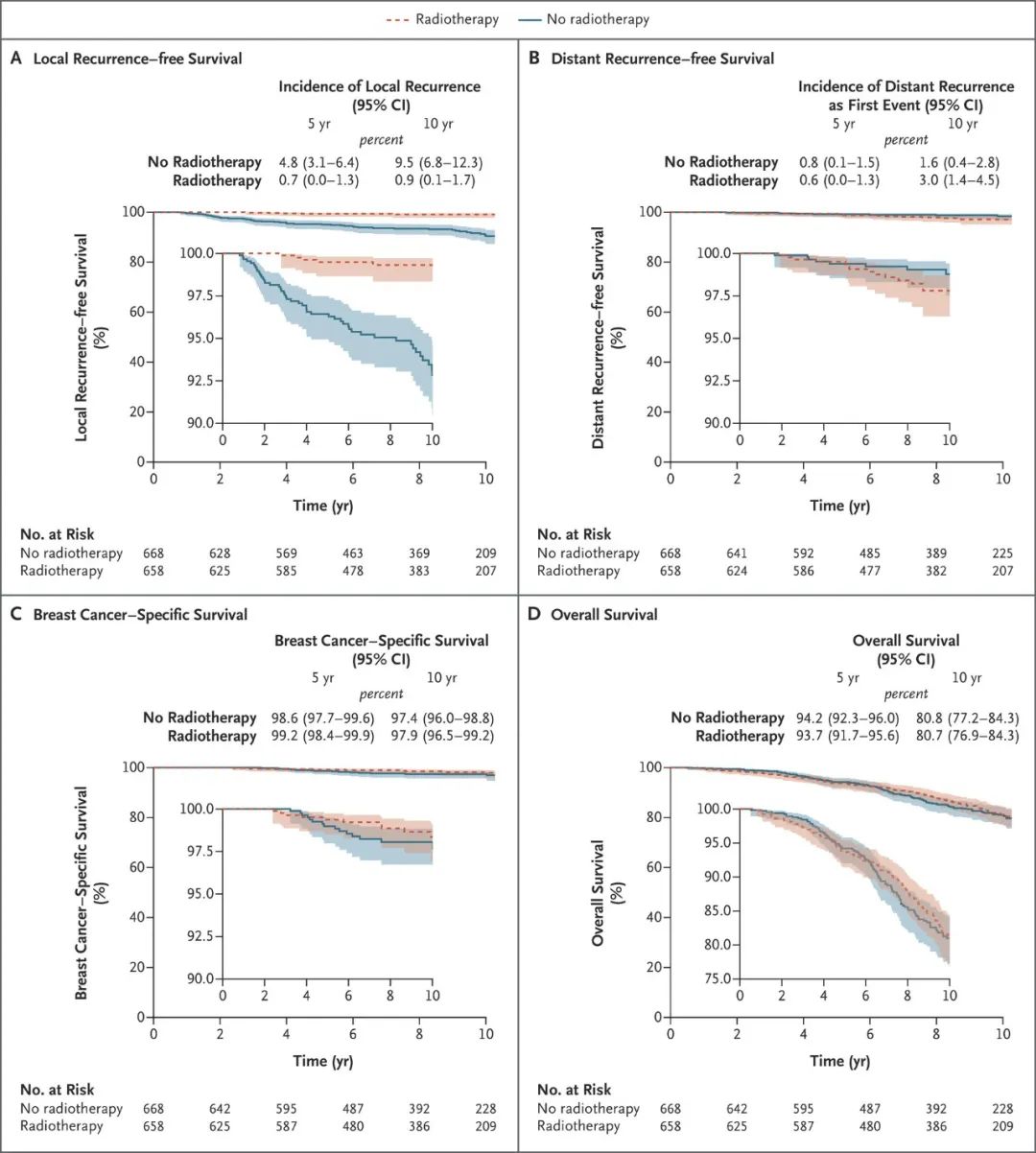
MP 低风险组的10年DMFI为98%,MP 高风险组为90%(p=0.011)。
MP LNUL和UL组在单独使用ET治疗的10年DMFI分别为99%和100%,表明MP LR组患者单独使用ET治疗时具有良好的长期预后。MP高风险组的患者预后较差,其中接受CT±ET治疗队列的10年DMFI为87%。
在≤50岁且MP风险为LNUL的患者,所有DMFI事件都发生在5年后。
研究结论
10年随访数据显示:MammaPrint极低风险单独接受ET的的患者预后良好,因此这些患者可以安全地缩短ET治疗时间。MammaPrint低风险但非极低风险(LNUL)组患者的大多数DMFI事件发生在5年后,这表明这些患者可能需要延长ET,这与NSABP-B42和IDEAL试验的观察结果一致。
MammaPrint检测联合转录组可更早提示新辅助内分泌治疗疗效
P5-09-02 Impact of neoadjuvant endocrine therapy on tumor transcriptome in patients with earlystage breast cancer from the FLEX trial
研究背景
新辅助内分泌治疗(NET)较少用于乳腺癌的常规治疗,除非患者合并多种疾病或者是不适合化疗的老年患者。NET的临床反应通常要在治疗几个月后才能达到。接受NET治疗2-4周后Ki67的降低(< 10%)被用作治疗有效的预测指标,但目前尚不确定单个基因或蛋白质是否可以充分预测预后或说明NET如何改变各种癌症基因和肿瘤生物学。
本研究通过比较NET前后匹配的肿瘤样本的全转录组基因表达变化,评估短期NET对早期乳腺癌(EBC)患者肿瘤基因组学的影响。
研究概览
患者情况:这项单中心FLEX子研究于2019年至2021年间入组30名至少接受两周的NET治疗HR+ HER2- EBC患者,采集了患者治疗前后匹配样本(绝经前妇女和1名男性乳腺癌患者接受Tamoxifen/ target=_blank class=infotextkey>他莫昔芬治疗(n=10),绝经后妇女接受来曲唑(n=10)或依西美坦治疗(n=10))并进行免疫组化(IHC)表达水平检测。
基因组检测:MammaPrint将肿瘤分为远处转移低风险或高风险。BluePrint和MammaPrint将肿瘤分为Luminal A型(MP 低风险)、Luminal B型(MP 高风险)、HER2阳性型或基底样basal型。
研究结果
在短期NET后乳腺肿瘤组织中检测到774个差异表达基因(DEGs) (图1A-B)。大多数DEGs(748个)下调,并与MYC和MTORC1信号传导、代谢、细胞增殖和上皮间充质转化相关(图1C)。NET后肿瘤中的上调基因,如FOS、JUN和EGR1与更好的预后相关。
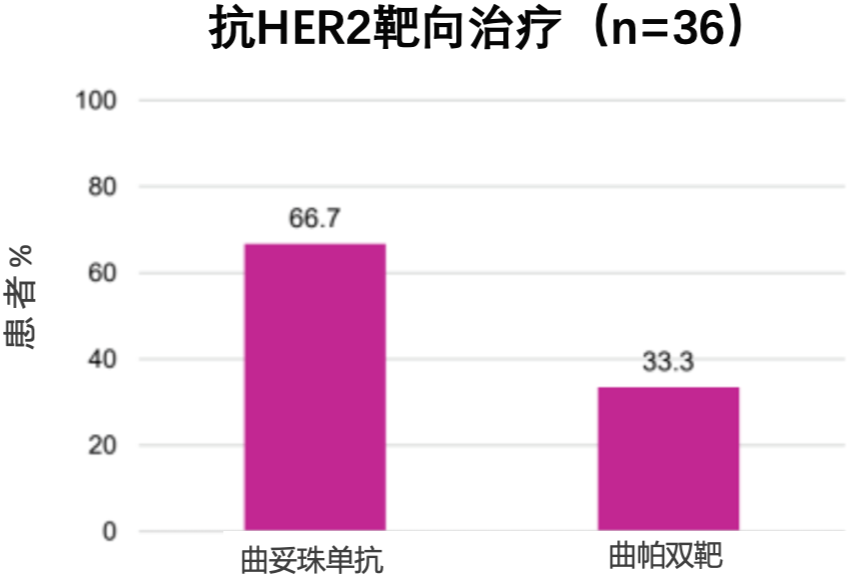
在NET后,30例患者的BluePrint分类没有变化(29例Luminal型和1例基底样型)。而MammaPrint评分显著升高,呈现向低风险转化的趋势。在NET后进行MammaPrint风险分层的重新评估,有6名患者从高风险变为低风险(图2A)。NET后的样本中“雌激素早期反应”的下调进一步支持了这一发现(图2B)。
在NET前后匹配的组织中,免疫组化中位数变化,ER为2.5%(p=0.750),PR为22%(p=0.097),Ki67为9%(p=0.026)(图3)。
研究结论
在这项研究中,与通常接受NET治疗后观察到的临床反应相比,可以在更短的时间内发现显著的基因表达变化。这可能表明生物学的复杂性和不同反应通路的多样性,通过整个转录组分析和MammaPrint检测比单一的IHC生物标志物更好地检测到这一点,尽管ER阳性百分比变化不大,但ER通路的下调也证明了这一点。
小 结
本文中的三项研究均揭示了70基因MammaPrint检测在预测内分泌延长治疗(EET)疗效、指导精准的内分泌治疗决策中发挥着重要作用。
第一项IDEAL研究中使用MammaPrint可以有效识别能从5年EET中获益的HR+、绝经后乳腺癌患者,研究发现与2.5年EET相比,接受5年EET的MammaPrint低风险(non-Ultralow)患者显示出绝对获益。然而MammaPrint高风险患者不能从EET中获益,或许可以避免过度的内分泌治疗。
第二项长达10年随访时间的研究结果显示:单独接受ET的MammaPrint超低风险患者预后良好,表明这些患者可以安全地缩短ET疗程,实现治疗降级。另外,MammaPrint低风险但非极低风险(LNUL)组患者更多的DMFI发生在5年后,表明这些患者需要延长ET疗程,加强治疗依从性,这与NSABP-B42和IDEAL试验的观察结果一致。
第三项研究中,与单一的IHC生物标志物相比,全转录组分析联合MammaPrint检测能在更短时间内观察到新辅助内分泌治疗(NET)的临床应答。这项研究表明MammaPrint可能有助于为接受NET的患者辅助确定术后治疗决策。
未来,期待更多前瞻性、多中心大样本研究对以上结果进行验证。